Основным процессом получения низших олефинов (этилена и пропилена) в настоящее время служит процесс термического пиролиза газового и жидкого углеводородного сырья (этана, ШФЛУ, бензиновых фракций) в трубчатых печах в присутствии водяного пара. Данный процесс имеет ряд недостатков, к которым относят использование высоких температур для эффективной конверсии сырья, многостадийность разделения продуктов реакции, а также при высоких температурах из-за высокой активности внутренних поверхностей пирозмеевиков, изготовленных из хромоникелевых сплавов, идет интенсивное коксоотложение, что приводит к значительному снижению времени работы пиролизных печей, и образовавшийся кокс трудно поддается удалению из пирозмеевиков и ЗИА при выжиге аппаратов.
Тем не менее производство этилена пиролизом в настоящее время находится на подъеме и продолжает расти в значительной степени, при этом объемы производства увеличиваются с каждым годом. В период с 1997 по 2021 год мировые мощности по производству этилена увеличились с 85 млн т/год до значений выше 150 млн т/год.
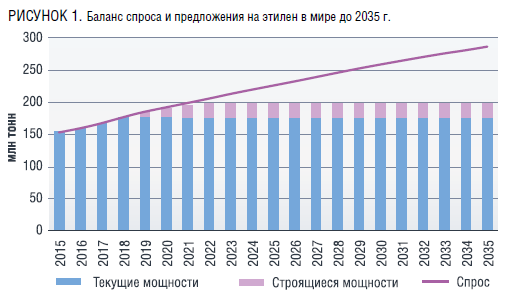
Структура ввода мировых мощностей по производству этилена напрямую связана с изменениями спроса и предложения, вызванными динамичностью и цикличностью развития мировой экономики, а темпы роста спроса на продукцию нефтехимии в мире существенны [1]. Так, среднегодовые темпы роста потребления полиэтилена составят 2,9 % в ближайшие 15 лет, что значительно превосходит темпы роста спроса на нефть (0,8 %) и газ (1,7 %). При этом предложение пока не поспевает за ростом спроса (рисунок 1). Уже в 2023 году планируемая потребность в полиолефинах достигнет более 210 млн т в год, а производительность имеющихся и строящихся установок прогнозируется на уровне менее 200 млн т. Это создает определенный дефицит на рынке и способствует рассмотрению реализации новых проектов, поэтому потенциальная производительность комплексов, по которым еще не принято инвестиционное решение, к 2035 году прогнозируется на уровне около 90 млн т.
Что касается России, с одной стороны, она обладает уникальной сырьевой базой для развития нефтехимии, являясь страной с крупнейшими запасами природного газа в объеме более 70 трлн м3 и занимающей шестое место в мире по запасам нефти, которые составляют около 15 млрд т, однако, с другой стороны, доля нашей страны на мировом рынке нефтегазохимии не превышает 2 %.
Производственные мощности пиролиза в России по состоянию на 2022 год составляют немногим более 4 млн т, при этом в течение последних 25 лет был введен в строй только один новый крупный пиролизный комплекс (ЗапСибНефтеХим), долгое время прирост производства этилена осуществлялся исключительно за счет модернизации и строительства новых печей на существующих предприятиях. Таким образом, номинальной мощности установок пиролиза недостаточно для переработки имеющегося сырья, что ведет к неудовлетворенности спроса на продукцию нефтехимии и как результат, темпы роста производства нефтехимической продукции в России значительно отстают от мировых.
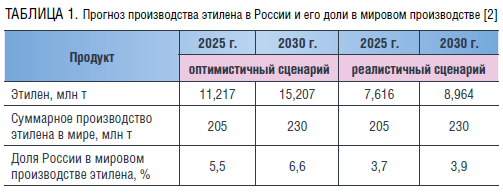
Согласно Плану развития нефтегазохимической отрасли РФ до 2030 года, в стране планируется создание шести нефтегазохимических кластеров, расположенных вблизи источников сырья и рынков сбыта: Северо-Западный, Волжский, Западно-Сибирский, Каспийский, Восточно-Сибирский и Дальневосточный [2]. Если план будет реализовываться, то уже в ближайшее время пиролизные мощности вырастут в 1,5 раза (таблица 1). Помимо этого, план устанавливает целевые показатели для отечественной нефтегазохимии по производству этилена и его доли в мировом производстве. Так, отечественные компании должны суммарно производить этилена, в соответствии с утвержденными целевыми показателями, более 7,5 млн т ежегодно, заняв более 3 % доли в мировом рейтинге [2].
Учитывая наличие неудовлетворенного спроса, все больше компаний рассматривают в своих R&D отделах окислительное дегидрирование как альтернативный способ получения не только олефинов С3 и С4, но и С2, несмотря на наличие некоторых проблем, основными из которых являются малая реакционная активность низших парафинов, а также высокая температура процесса [3]. Использование окислительного способа дегидрирования позволяет снизить температуру процесса, а кислород препятствует обратимости процесса из-за образования водяного пара с выделяющимся водородом. Тем не менее данная особенность обуславливает выделение тепла, что делает актуальной проблему отвода или компенсации избыточной энергии, выделяемой в ходе реакции. Однако если каталитическое дегидрирование парафинов широко используется для получения олефинов еще с 60-х годов прошлого века, то полученные к настоящему времени результаты по окислительному дегидрированию одного из самых инертных парафинов этана (что наиболее интересно для окислительного дегидрирования) пока еще недостаточно актуальны для промышленной реализации.
В настоящее время перспективы процесса окислительного дегидрирования этана рассматриваются через призму разработки новых каталитических систем и оптимизации известных. Значительное внимание уделяется поискам систем с использованием оксидных катализаторов на основе молибдена и ванадия с нанесением на различные носители, так как для промышленных высокотемпературных каталитических процессов характерно именно применение активных компонентов, например, смешением.
Каталитическое дегидрирование алканов применяется в промышленности с 1930-х годов [4]. Сильно эндотермический и ограниченный равновесием процесс выполняется в реакторах с неподвижным слоем, поэтому следует обеспечивать высокие температуры и низкое давление в реакционном пространстве в силу термодинамики процесса [5]. Например, для достижения равновесных конверсий этана более 40 % при атмосферном давлении температуры реакции должны быть более 700 °С, а высокое давление процесса сдвигает равновесие в сторону сырья.
Часто используемыми катализаторами процесса являются соединения на основе хрома (т.е. хром на γ-окиси алюминия) или платины. Основными проблемами дегидрирования являются подавление побочных реакций и синтез катализаторов подходящей формы в виде гранул, обеспечивающих эффективное распределение сырья и минимизирующих перепад давления. Последовательные побочные реакции приводят к образованию диенов, полимеров и кокса и, следовательно, требуется частая регенерация катализатора для поддержания приемлемого срока службы, для чего применяется окислительная регенерация (воздухом или смесью воздух-дымовые газы) [6].
Одним из первых коммерческих процессов дегидрирования является Катадиен, в котором применяется катализатор на основе оксида алюминия-хрома. Данный процесс был использован для производства бутадиена с использованием параллельного расположения реакторов с неподвижным слоем, которые работают в режиме чередования стадий дегидрирования и регенерации (удаление кокса).
В конце 1980-х разработка новых процессов расширила возможности производства пропилена из пропана. Процесс Catofin использует дегидрирование и регенерацию катализатора в режиме аналогичном процессу Катадиен [7]. Используется адиабатический тип реактора с неподвижным слоем Cr2O3/γ-Al2O3 катализатора, и предварительно нагретый пропан подается в реактор с охлаждением по мере протекания реакции вдоль реактора. Режим работы реактора – циклический. Время цикла «дегидрирование – регенерация» составляет 25 мин, температура процесса 525–677 °C. В результате конверсия пропана варьируется в пределах 48–65 %, селективность по пропилену – 82–87 %. В начале 1970-х годов UOP представила концепцию непрерывного времени цикла «дегидрирование – регенерация» (CCR). В соответствующем процессе использовался адиабатический реактор с движущимся слоем Pt-Sn-K/γ-Al2O3 катализатора (UOP Oleflex) [8]. Температура процесса составляет 525–705 °C, конверсия пропана равна 25–40 %, селективность по пропилену 89–91 %. Однако дегидрирование этана с использованием данных процессов не может конкурировать с пиролизом из-за относительно низкой активности катализаторов (несущественный выход за один цикл).
В отличие от процессов дегидрирования и пиролиза, окислительное дегидрирование этана (ОДГЭ) еще не было осуществлено в производственных масштабах. Принципиальное преимущество перед дегидрированием заключается в высокой конверсии этана, потенциально более низкими температурами реакции (около 400–600 °С) по сравнению с пиролизом, и тот факт, что реакция является экзотермической, вызвало колоссальный интерес к этому процессу.
Низкомолекулярные алканы являются подходящим сырьем для окислительного дегидрирования, так как это достаточно дешевые углеводороды, которые добываются в больших количествах из природного и сланцевого газов. Стоит отметить, что процесс окислительного дегидрирования имеет принципиальные отличия от парового крекинга углеводородов. Во-первых, наличие кислорода требует обеспечения дополнительных мер безопасности для предотвращения неуправляемого горения и взрывоопасных смесей. Во-вторых, разработка подходящих катализаторов является особенно сложной, поскольку олефиновые продукты имеют тенденцию быть более реакционноспособными, чем алканы [9]. Эта высокая реакционная способность олефинов объясняется усилением дополнительного связывания с большинством каталитических поверхностей, тогда как алканы взаимодействуют почти исключительно посредством сил дисперсии.
В качестве окислителя может применяться как концентрированный кислород, так и кислород в составе воздуха:

Поскольку этан превращается в этен посредством дегидрирования, может происходить полное окисление, в результате которого образуются CO и CO2, а также вода. Практически полная селективность образования одного олефина возможна только с этаном в качестве исходного сырья, поскольку этилен является единственным возможным продуктом дегидрирования, и добавление кислорода не способствует образованию органических, кислородосодержащих соединений.
Целевая реакция окислительного дегидрирования этана протекает на поверхности катализатора. Предположительный механизм данной реакции включает в себя несколько стадий, лимитирующей обычно считается стадия активации этана с образованием этильного радикала, адсорбированного на поверхности катализатора:

Далее на катализаторах на основе оксидов переходных металлов реакция протекает по поверхностному механизму Марса-ван-Кревелена через промежуточное образование этокси-производных, причем среди кислородных форм, принимающих участие на этой стадии реакции, важную роль играют нуклеофильные ионы O2−, которые отдает катализатор для осуществления данного процесса:

С повышением температуры разложение этокси-производных до этилена оказывается более выгодным, чем их более глубокое окисление до оксидов углерода. Это согласуется с ростом селективности по этилену при увеличении температуры процесса:
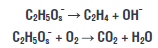
В теории реакция дегидрирования этана сопровождается многими параллельными и последовательными процессами, что может существенно влиять на равновесный состав и на выход этилена. При высоких температурах возможно образование радикальных соединений.
К числу наиболее перспективных катализаторов процесса окислительного дегидрирования относятся оксиды переходных металлов (V, Nb, Mo), нанесенные на оксид алюминия методом молекулярного наслаивания (МН). Этот метод основан на необратимом взаимодействии между низкомолекулярными реагентами и функциональными группами поверхности твердого субстрата в условиях непрерывной подачи реагента и удаления образующихся газообразных продуктов, позволяет получать структурированные многослойные каталитические системы разного состава и строения и влиять на активность и селективность катализатора. Выбор металлов в качестве катализаторов связан с большой активностью в реакции окислительного дегидрирования и их свойствами: ванадий отвечает за активацию исходной молекулы этана, а молибден – за селективность процесса по этилену. Ранее была показана возможность использования наноструктурированных катализаторов на основе Mo, Nb, V, Ti на оксиде алюминия, приготовленных методом МН, в реакции ОДГЭ [11].
Как правило, данная группа катализаторов работоспособна при температуре реакции ниже 600 °C и функционирует по окислительно-восстановительному механизму. В этой группе наиболее перспективными являются каталитические системы, содержащие ванадий, то есть оксиды металлов в смеси с ванадием; ванадий, нанесенный на оксиды металлов; V-содержащие микропористые/мезопористые материалы.
Mo–V–Nb-оксидные системы, используемые в реакции ОДГЭ, известны с 1970-х гг. [13]. На них при температурах менее 300 °C была достигнута достаточно высокая селективность образования этилена (70 %) при умеренной конверсии этана (20 %). Модифицирование теллуром позволило значительно повысить как активность (до 59 %), так и селективность (до 89 %) этих систем при 400 °C [14].
Особый интерес исследователей направлен на изучение и разработку нанесенных ванадиевых катализаторов ОДГЭ, высокие каталитические характеристики которых обусловлены состоянием ванадия, присутствующего в катализаторах в виде поверхностных изолированных и/или полимерных VOx форм.
В случае нанесенных V2O5/MgO катализаторов, считающихся одними из наиболее эффективных катализаторов ОДГЭ, в отличие от большинства других носителей (SiO2, TiO2, γ-Al2O3), отмечается образование не поверхностных VOx форм, а, по данным разных исследователей, слоев поверхностного V-Mg-O-соединения или каталитически активной дисперсной фазы Mg3V2O8. При этом ортованадат магния, диспергированный на поверхности MgO, высокоактивен в реакциях ОДГЭ, в то время как массивный Mg3V2O8 – практически неактивен. Работы по исследованию массивных образцов ванадатов магния различного состава (Mg3V2O8, MgV2O6 и Mg2V2O7) в качестве модельных катализаторов показывают, что их каталитические свойства изменяются в зависимости от состава и структуры ванадатов, а также реакционной способности УВ. Однако данные об исследованиях катализаторов на основе дисперсных MgV2O6 и Mg2V2O7, формирование которых на поверхности MgO затруднено, а также Mg3V2O8 на поверхности других носителей, практически отсутствуют.
Каталитические системы на основе никеля являются еще одним важным классом катализаторов ОДГЭ. Они также широко применяются и в других важных процессах, таких как гидрирование, риформинг природного газа для получения синтез-газа, деалкилирование и т.д. Никелевые катализаторы на основе оксида алюминия были испытаны в окислительном дегидрировании этана и показали хорошие результаты. Использование полиметаллического никеля оказывает большое влияние на способность катализаторов активировать молекулы этана и избирательно превращать их в этилен.
К числу наиболее перспективных катализаторов для ОДГЭ относятся оксиды V и Mo, нанесенные на Al2O3, TiO2, SiO2, MgO и ZrO2 [15]. Задача процесса сводится к достижению высокой конверсии и селективности по этилену, но большинство катализаторов ОДГЭ имеют свойство давать более термодинамически выгодные продукты (например, CO2) при высоких конверсиях. Совместная подача этана и O2 также требует разделения сепарации воздуха и дополнительных мер безопасности. В качестве альтернативы исследуются новые катализаторы типа «ядро-оболочка», которые работают в циклическом окислительно-восстановительном режиме, обеспечивая тем самым высокую селективность по отношению к этилену.
Несмотря на разработку большого количества каталитических систем, развитие процесса окислительного дегидрирования этана, как альтернативного способа производства этилена, является актуальной задачей, так как с каждым годом спрос на этилен в мире опережает его предложение на рынке. ОДГЭ позволяет существенно снизить температуру процесса получения этилена, что экономически оправдывает введение данного процесса в широкое применение.
В настоящее время развитие ОДГЭ направлено на поиск новых катализаторов. Каталитические системы на основе переходных металлов имеют преимущество и являются наиболее перспективными, с применением молибдена и ванадия были достигнуты наилучшие показатели по результатам каталитических исследований.
Работа выполнена в рамках специального именного гранта некоммерческой организации «Благотворительный фонд «ЛУКОЙЛ»






